Sociedad -
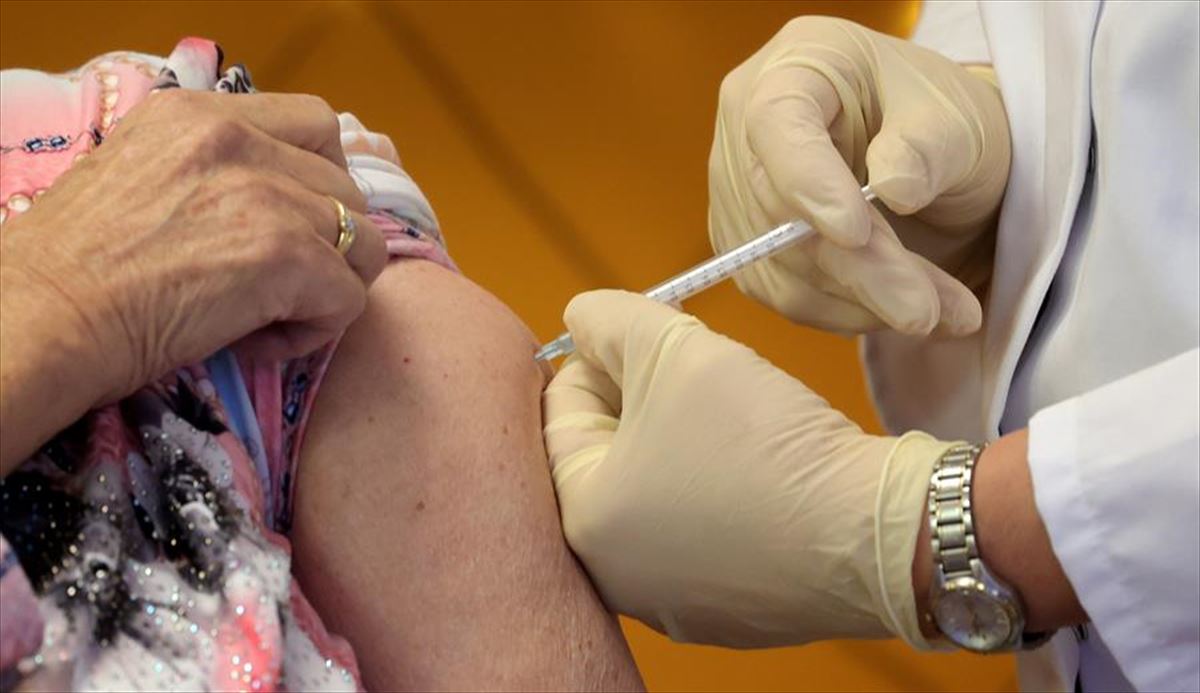
VACUNACIÓN
Biocruces y Biodonostia comienzan a reclutar voluntarios para los ensayos de Curevac
Para participar en el ensayo se debe completar un formulario de preinscripción a partir de hoy, con datos básicos de identidad y un contacto, que se podrá rellenar a través de internet.

L.Z. | EITB MEDIA
Euskaraz irakurri: Curevacen entseguetarako boluntarioak hartzen hasi dira Biocruces eta Biodonostia
Los institutos de investigación sanitaria Biocruces y Biodonostia han comenzado este viernes el proceso para reclutar voluntarios para los ensayos clínicos de la vacuna contra la covid-19 desarrollada por el laboratorio alemán Curevac.
Para participar en el ensayo se debe completar un formulario de preinscripción a partir de hoy, con datos básicos de identidad y un contacto, que se podrá rellenar a través de internet, tal y como se explicaba en una cadena de whatsapp puesta en circulación desde Biodonostia.
Se trata de un ensayo clínico en el que participarán 30 000 personas de todo el mundo, de las que hasta 2000 podrían ser vascos mayores de 18 años, que recibirán dos dosis de la vacuna con un intervalo de 28 días.
Curevac ha desarrollado una vacuna basada en el mecanismo del RNA mensajero que estimula el sistema inmunitario, es decir, el mismo que emplean las dos vacunas que se están distribuyendo actualmente de Pfizer y Moderna.
Sin embargo, las condiciones de mantenimiento y preparación de la vacuna de Curevac "facilitan la logística de su distribución", que hasta ahora es "uno de los principales obstáculos". Además, al producirse en Europa es una de las vacunas que más dosis ha comprometido para su distribución en este continente.
Pueden participar en el estudio las personas mayores de 18 años que cumplan los criterios señalados en el protocolo del estudio.
Las personas seleccionadas serán distribuidas de forma aleatoria en el grupo que recibe la vacuna o en el de control que recibe un placebo sin ningún efecto. El ensayo requiere dos dosis inoculadas con 28 días de margen.
Las personas participantes recibirán un seguimiento de hasta un año con visitas médicas y llamadas telefónicas y además contarán con una aplicación móvil que facilitará el registro de la información. Estos voluntarios podrán solicitar abandonar en cualquier momento y conocer si recibieron vacuna o placebo
A los tres y a los seis meses desde la administración de la vacuna se les harán análisis intermedios y, en función de los resultados, se podría acelerar la aprobación del uso de la vacuna como ha ocurrido con algunas de las ya comercializadas.